 Forskere indsatte et gen for en grøn lysreceptor i øjnene på blinde mus, og en måned senere navigerede musene lige så let omkring forhindringer som dem uden synsproblemer.
Forskere indsatte et gen for en grøn lysreceptor i øjnene på blinde mus, og en måned senere navigerede musene lige så let omkring forhindringer som dem uden synsproblemer.
Musene kunne se bevægelse, lysstyrkeændringer over tusind gange og fine detaljer på en iPad tilstrækkelig til at skelne mellem bogstaver.
Forskerne siger, at inden for så lidt som tre år kunne genterapi - som de leverede via en inaktiv virus - gå til test hos mennesker, der har mistet synet på grund af retinal degeneration, hvilket ideelt set giver dem nok syn til at bevæge sig rundt og potentielt gendanne deres evne til at læse eller se en video.
"Du ville injicere denne virus i en persons øje, og et par måneder senere ville de se noget," siger Ehud Isacoff, professor i molekylær og cellebiologi ved University of California, Berkeley, og direktør for Helen Wills. Neuroscience Institute.
"... hvor vidunderligt ville det være for blinde mennesker at genvinde evnen til at læse en standard computerskærm, kommunikere via video, se en film."
”Med neurodegenerative sygdomme i nethinden forsøger ofte alle mennesker at stoppe eller bremse yderligere degeneration. Men noget, der gendanner et billede om få måneder - det er en fantastisk ting at tænke på. ”
Omkring 170 millioner mennesker over hele verden lever med aldersrelateret makuladegeneration, som rammer en ud af 10 personer over 55 år, mens 1.7 millioner mennesker verden over har den mest almindelige form for arvelig blindhed, retinitis pigmentosa, som typisk efterlader folk blinde efter alderen af 40.
”Jeg har venner uden lysopfattelse, og deres livsstil er hjertesværgende,” siger John Flannery, professor i molekylær og cellebiologi, der er på fakultetet for School of Optometry.
”De er nødt til at overveje, hvad seende mennesker tager for givet. For eksempel, hver gang de går til et hotel, er hvert rumlayout lidt anderledes, og de har brug for nogen til at gå dem rundt i lokalet, mens de bygger et 3D-kort i hovedet. Hverdagsgenstande, som et lavt sofabord, kan være en fare for at falde. Sygdomsbyrden er enorm blandt mennesker med alvorligt nedsat synstab, og de kan være de første kandidater til denne form for terapi. ”
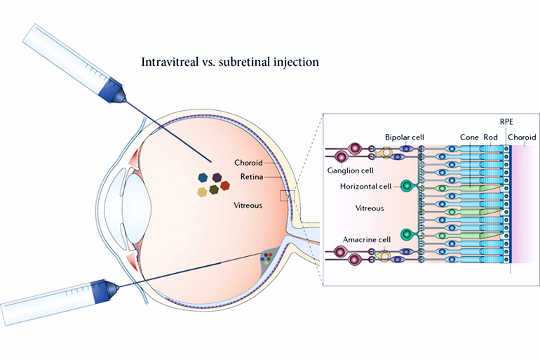 Den nye terapi involverer injektion af inaktiverede vira i glaslegemet for at bære et gen direkte ind i ganglionceller. Tidligere versioner af viral terapi krævede injektion af vira under nethinden (nederst). (Kredit: John Flannery)
Den nye terapi involverer injektion af inaktiverede vira i glaslegemet for at bære et gen direkte ind i ganglionceller. Tidligere versioner af viral terapi krævede injektion af vira under nethinden (nederst). (Kredit: John Flannery)
I øjeblikket er mulighederne for sådanne patienter begrænset til et elektronisk øjenimplantat, der er tilsluttet et videokamera, der sidder på et par briller - et akavet, invasivt og dyrt setup, der producerer et billede på nethinden, der i øjeblikket svarer til et par hundrede pixels. Normal, skarp vision involverer millioner af pixels.
Korrigering af den genetiske defekt, der er ansvarlig for retinal degeneration, er heller ikke ligetil, fordi der er mere end 250 forskellige genetiske mutationer, der er ansvarlige for retinitis pigmentosa alene. Omkring 90 procent af disse dræber nethindens fotoreceptorceller - stængerne, der er følsomme over for svagt lys og keglerne for dagslysfarveopfattelse. Men retinal degeneration skåner typisk andre lag af retinalceller, herunder de bipolare og retinal ganglionceller, som kan forblive sunde, skønt de er ufølsomme over for lys, i årtier efter at folk bliver helt blinde.
I deres forsøg med mus lykkedes det forskerne at gøre 90 procent af ganglionceller lysfølsomme.
Et simpelt system
For at vende blindhed hos disse mus designede forskerne en virus målrettet mod retinale ganglionceller og fyldte den med genet til en lysfølsom receptor, den grønne (medium bølgelængde) kegleopsin. Normalt kun kegle fotoreceptorceller udtrykker denne opsin, og det gør dem følsomme over for grønt-gult lys. Da forskere injicerede det i øjet, førte virussen genet ind i ganglionceller, som normalt er ufølsomme over for lys, og gjorde dem lysfølsomme og i stand til at sende signaler til hjernen, som den fortolkede som syn.
"Til de grænser, at vi kan teste musene, kan du ikke fortælle de optogenetisk behandlede muses opførsel fra de normale mus uden specielt udstyr," siger Flannery. "Det er tilbage at se, hvad det oversætter til hos en patient."
Hos mus leverede forskerne opsins til de fleste ganglionceller i nethinden. For at behandle mennesker er de nødt til at injicere mange flere viruspartikler, fordi det menneskelige øje indeholder tusinder af gange flere ganglionceller end musens øje. Men holdet har udviklet midlerne til at forbedre viral levering og håber at indsætte den nye lyssensor i en tilsvarende høj procentdel af ganglionceller, et beløb svarende til de meget høje pixeltal i et kamera.
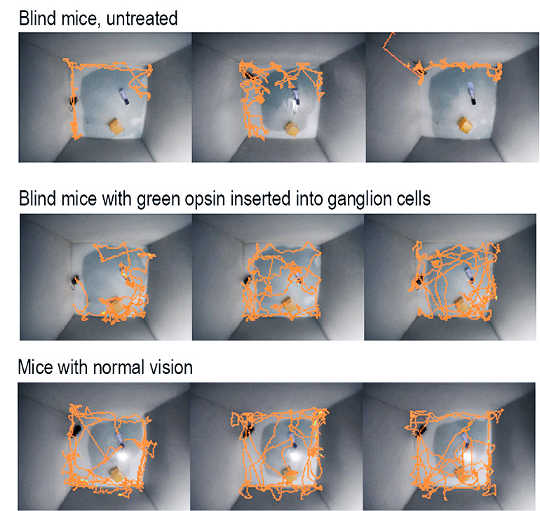 De orange linjer sporer musernes bevægelse i det første minut, efter at forskerne satte dem i et mærkeligt bur. Blinde mus (øverst) holder sig forsigtigt i hjørnerne og siderne, mens behandlede mus (i midten) udforsker buret næsten lige så meget som normalt synede mus (nederst). (Kredit: Ehud Isacoff / John Flannery)
De orange linjer sporer musernes bevægelse i det første minut, efter at forskerne satte dem i et mærkeligt bur. Blinde mus (øverst) holder sig forsigtigt i hjørnerne og siderne, mens behandlede mus (i midten) udforsker buret næsten lige så meget som normalt synede mus (nederst). (Kredit: Ehud Isacoff / John Flannery)
Isacoff og Flannery kom på den enkle løsning efter mere end et årti med at prøve mere komplicerede ordninger, herunder indsættelse i overlevende retinalceller kombinationer af genetisk konstruerede neurotransmitterreceptorer og lysfølsomme kemiske switches. Disse fungerede, men opnåede ikke følsomheden af normalt syn. Opsins fra mikrober testet andetsteds havde også lavere følsomhed, hvilket krævede brug af lysforstærkende beskyttelsesbriller.
For at fange den høje følsomhed af naturlig syn vendte forskerne sig mod lysreceptoropsins fra fotoreceptorceller. Ved hjælp af en adeno-associeret virus, der naturligt inficerer ganglionceller, leverede de genet med succes til et retinal opsin i genomet af ganglioncellerne. De tidligere blinde mus fik syn, der varede hele livet.
”At dette system fungerer er virkelig, virkelig tilfredsstillende, dels fordi det også er meget simpelt,” siger Isacoff. "Ironisk nok kunne du have gjort dette for 20 år siden."
Forskerne skaffer midler til at tage genterapien ind i et forsøg på mennesker inden for tre år. Lignende AAV-leveringssystemer er godkendt af FDA til øjensygdomme hos mennesker med degenerative retinale tilstande, og som ikke har noget medicinsk alternativ.
Trods oddsene
Ifølge Flannery og Isacoff ville de fleste mennesker i synsfeltet stille spørgsmålstegn ved, om opsins kunne arbejde uden for deres specialiserede stang- og kegle fotoreceptorceller. Overfladen på en fotoreceptor er dekoreret med opsins - rhodopsin i stænger og røde, grønne og blå opsins i kegler - indlejret i en kompliceret molekylær maskine. Et molekylært relæ - den G-proteinkoblede receptorsignaleringskaskade - forstærker signalet så effektivt, at vi er i stand til at detektere enkelte lysfotoner.
Et enzymsystem genoplader opsinet, når det registrerer fotonet og bliver ”bleget”. Feedbackregulering tilpasser systemet til meget forskellige baggrundslysstyrker. Og en specialiseret ionkanal genererer et kraftigt spændingssignal. Uden at transplantere hele dette system var det rimeligt at mistanke om, at opsinet ikke ville fungere.
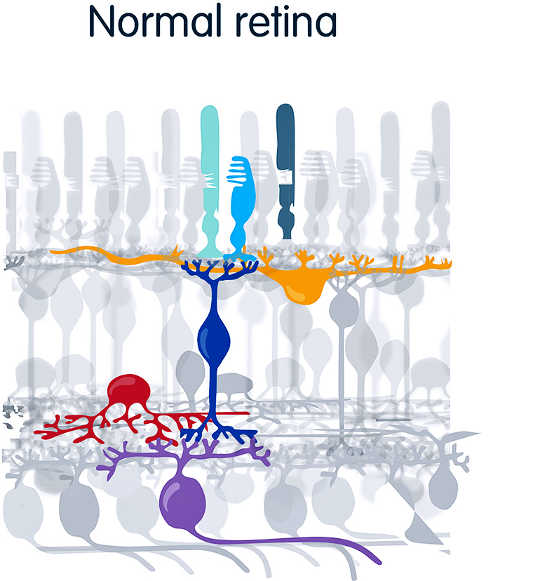 I en normal nethinde registrerer fotoreceptorer - stænger (blå) og kegler (grøn) - lys- og relæsignalerne til andre lag i øjet, der ender i ganglioncellerne (lilla), der taler direkte til hjernens synscenter. (Kredit: UC Berkeley)
I en normal nethinde registrerer fotoreceptorer - stænger (blå) og kegler (grøn) - lys- og relæsignalerne til andre lag i øjet, der ender i ganglioncellerne (lilla), der taler direkte til hjernens synscenter. (Kredit: UC Berkeley)
Men Isacoff, der specialiserer sig i G-proteinkoblede receptorer i nervesystemet, vidste, at mange af disse dele findes i alle celler. Han mistænkte, at en opsin automatisk ville oprette forbindelse til signalsystemet i retinale ganglionceller. Sammen forsøgte han og Flannery oprindeligt rhodopsin, som er mere følsom over for lys end kegleopsins.
Da de introducerede rhodopsin i ganglioncellerne hos mus, hvis stænger og kegler var helt degenereret, og som følgelig var blinde, genvandt dyrene deres glæde evnen til at fortælle mørkt fra lys - endog svagt rumlys. Men rhodopsin viste sig at være for langsom og mislykkedes i genkendelse af billeder og objekter.
De prøvede derefter den grønne kegleopsin, som reagerede 10 gange hurtigere end rhodopsin. Bemærkelsesværdigt var musene i stand til at skelne parallelt fra vandrette linjer, linjer tæt fordelt versus bredt adskilt (en standard menneskelig skarphedsopgave), bevægelige linjer versus stationære linjer. Den gendannede vision var så følsom, at iPads kunne bruges til de visuelle skærme i stedet for meget lysere lysdioder.
”Dette bragte meddelelsen kraftigt hjem,” siger Isacoff. "Når alt kommer til alt, hvor vidunderligt det ville være for blinde mennesker at genvinde evnen til at læse en standard computerskærm, kommunikere via video, se en film."
Disse succeser fik Isacoff og Flannery til at gå et skridt videre og finde ud af, om dyr kunne navigere i verden med gendannet syn. Påfaldende nok var også den grønne kegleopsin en succes. Mus, der havde været blinde, genvandt deres evne til at udføre en af deres mest naturlige adfærd: genkendelse og udforskning af tredimensionelle objekter.
De stillede derefter spørgsmålet: ”Hvad ville der ske, hvis en person med gendannet syn gik udendørs i lysere lys? Ville de blive blændede af lyset? ” Her opstod et andet slående træk ved systemet, Isacoff siger: Den grønne kegle opsin signalveje tilpasser sig. Dyr, der tidligere var blinde justeret til lysstyrkeændringen og kunne udføre opgaven lige så godt som seende dyr. Denne tilpasning fungerede over en rækkevidde på omkring tusind gange - forskellen i det væsentlige mellem gennemsnitlig indendørs og udendørs belysning.
"Når alle siger, at det aldrig vil fungere, og at du er skør, betyder det normalt, at du er på noget," siger Flannery. Faktisk svarer det til den første vellykkede gendannelse af mønstret syn ved hjælp af en LCD-computerskærm, den første til at tilpasse sig ændringer i omgivende lys og den første til at gendanne det naturlige objektsyn.
Forskningen vises i Nature Communications. Holdet arbejder nu på at teste variationer på temaet, der kan gendanne farvesyn og øge skarpheden og tilpasningen yderligere. National Eye Institute of the National Institutes of Health, Nanomedicine Development Center for the Optical Control of Biological Function, Foundation for Fighting Blindness, Hope for Vision Foundation og Lowy Medical Research Institute støttede forskningen.
Kilde: UC Berkeley
Relaterede bøger
at InnerSelf Market og Amazon






















